Première pandémie respiratoire de l’ère industrielle
Un coronavirus en serait-il responsable ?
12 janvier 1890
En guise d'introduction
En m’intéressant récemment aux peintres impressionnistes, et en particulier à Berthe Morisot, j’apprends qu’elle serait décédée de la grippe à 54 ans, en mars 1895. Son époux Eugène, le frère cadet d’Edouard Manet, serait décédé 3 ans plus tôt, en avril 1892, de syphilis pulmonaire. Son frère Edouard est d’ailleurs également mort en 1883, atteint du stade 3 de la syphilis qu’il a contractée très jeune, pendant les quelques années passées dans la marine militaire. Comme Baudelaire ou Rimbaud plus tard, il meurt d’ataxie locomotrice, une attaque des muscles et tendons des jambes, due à l’atteinte du système nerveux par la syphilis. La syphilis était extrêmement répandue aux XVIIIe et XIXe siècles, et le seul traitement était les sels de mercure, en réalité totalement inefficaces, si bien que la toute grande majorité des personnes atteintes atteignait le stade 3, qui attaquait divers organes, mais très particulièrement le système nerveux et le système cardiovasculaire.
Berthe Morisot avait fréquenté Edouard Manet pendant 15 ans avant son mariage avec son frère cadet. Berthe Morisot fut le modèle qu’Edouard Manet a le plus souvent représenté sur ses toiles, parfois dans des poses très lascives dans l’atelier de Manet. Il n’y a aucune preuve qu’il y ait eu une réelle relation entre Berthe Morisot et Edouard Manet, mais c’est hautement probable. D’abord en considérant le côté très intime de certaines toiles de Manet, le petit bouquet de violettes peint pour elle alors qu’elle se fiance avec son frère, et qu’il lui dédicace (en langage des fleurs, les violettes traduisent la profondeur des sentiments), et enfin, alors que Berthe Morisot entreprenait une correspondance prolifique avec tous ses amis, aucune correspondance n’a été retrouvée entre elle et Edouard Manet, laissant penser que cette correspondance a été détruite, pour ne pas laisser d’indices.

Edouard Manet et son frère étant tous deux syphilitiques, il me semble vraisemblable que Berthe Morisot ait été également contaminée et qu’elle en souffrait. Elle se plaignait depuis la fin des années ’80 déjà, du fait qu’Eugène et elle, vieillissaient prématurément et d’être en permanence fatiguée. Comme on l’a dit, Eugène meut en 1892, à 58 ans, de ce qu’on a appelé une syphilis pulmonaire. Mais j’ai cherché dans la littérature relative à la syphilis, et je n’ai trouvé aucune description particulière d’une forme pulmonaire de la syphilis. Par contre, à un stade avancé, il est certain que la syphilis affaiblit l’organisme de façon extrême et rend le malade particulièrement sensible aux infections. De même, en 1795, à 54 ans, Berthe Morisot meurt de la grippe, après en avoir soigné sa fille Julie. Dans les deux cas, ils sont emportés par ce qui fut sans doute des pneumopathologies, dues à la grippe ou à une autre affection respiratoire, s’aggravant chez deux personnes particulièrement affaiblies. Était-ce la grippe ou une autre affection ?
La grippe dans la dernière décennie du XIXe siècle.
Après une pandémie de grippe en 1847-48, la grippe saisonnière a ensuite été très peu active dans les décennies suivantes, jusqu’à soudainement réapparaître pendant l’hiver 1889-90, en prenant la forme d’une pandémie, venue du centre de la Russie, plus précisément de Boukhara, alors dans le Turkestan, et qui allait faire le tour du monde, très rapidement, en profitant du chemin de fer et des bateaux à vapeur qui avaient fait leur apparition. De par son origine, cette pandémie s’est appelée le « Grippe russe ». Elle a fait des centaines de milliers de victimes cette année-là. Et la seconde vague de 1991 en fera encore davantage. Au total, les estimations font état d’un million de décès, chiffre très certainement sous-estimé en raison d’un manque de données ou de registres d’état civil dans de nombreux pays. La population mondiale est alors d’un milliard et demi d’habitants. Ramené à la population mondiale d’aujourd’hui, cela correspondrait donc à au moins 5 millions de victimes. Un nombre similaire à la pandémie de SARS-CoV-2 d’aujourd’hui. Mais cependant nettement inférieur au 50 à 100 millions de victimes de la grippe espagnole de 1918-1921.
De fortes vagues épidémiques ont encore suivi tout au long de cette décennie, principalement en 1892 jusqu’au printemps 1995 et ensuite surtout en 1899-1900, sans toutefois qu’on puisse être sûr qu’il s’agisse toujours du même pathogène. La connaissance scientifique a évolué en cette fin de siècle, et on connaît l’existence de « germes », c’est à dire de microbes, se transmettant de personne à personne, grâce notamment à l’observation du bacille de Koch, au lieu des « miasmes », ainsi qu’on l’a cru longtemps jusque-là, c’est à dire d’agents nocifs provenant spontanément de l’air vicié. Toutefois, la notion de virus est encore totalement inconnue. Et de même qu’on a longtemps confondu épidémies de peste et de choléra, les maladies provoquant toux, fièvre, douleurs musculaires et articulaires et pouvant conduire parfois à des cas de détresse respiratoire, sans qu’aucun agent pathogène causal ne puisse être détecté, étaient d’office imputées à la grippe. Quel que soit l’agent pathogène, c’est très probablement deux de ces vagues importantes de « grippe » qui ont emporté d’abord Eugène Manet, et trois ans plus tard, Berthe Morisot.
Arguments en faveur d’une pandémie de grippe
Quatre espèces de virus de grippe différents sont connus, A, B, C et D ( pour Alphainfluenza, Betainfluenza, etc. ). Ceux responsables de la grippe humaine sont essentiellement de type A et B. Tous les virus de grippe sont des virus à ARN, et non à ADN. L’ARN étant beaucoup plus fragile que l’ARN, cela explique que la grippe mute très fréquemment. Dans tous les cas, l’ARN des virus de grippe est monocaténaire, ce qui signifie qu’il est constitué d’un seul brin, et pas de deux brins entrelacés comme c’est le cas pour l’ADN en général, et en particulier dans le patrimoine génétique humain, contenu dans le noyau de nos cellules.
Non seulement, le virus de la grippe est constitué d’un seul brin d’ARN, mais celui-ci est de plus segmenté en plusieurs morceaux. Ainsi, le virus A est segmenté en 8 morceaux. Cette segmentation augmente les possibilités de réarrangement entre deux souches de virus d’une même espèce (virus se différentiant par un ensemble de mutations). De plus, l’ARN des virus de la grippe est à polarité négative, ce qui veut dire qu’il ne peut pas être directement lu par les usines à protéines de nos cellules (les ribosomes), mais doivent d’abord être répliqués en leur ARN complémentaire, qui lui, pourra être lu. Cette étape complémentaire de réplication est bien sûr une source potentielle d’erreurs supplémentaires, donc de mutations.
Les virus humains A et B ont tous deux, deux protéines de surfaces caractéristiques et qui jouent un rôle crucial dans le mécanisme de reproduction du virus : ce sont l’hémagglutinine, d’une part, abréviée en H, et la neuraminidase d’autre part, abréviée en N.
Ces protéines subissant des mutations, on distingue, dans l’évolution de ces virus, de nombreux sous-types, particulièrement nombreux pour l’espèce B, moins nombreuses pour l’espèce A. Mais si l’espèce B est responsable très souvent d’épisodes de grippes saisonnières, tout comme la grippe A, ce sont toujours des nouveaux sous-types émergeants de l’espèce A qui ont été responsables des pandémies de grippe. Les pandémies sont dues à l’émergence de nouveaux sous-types d’hémagglutinine H, ou à la réapparition de celui-ci après une très longue période de disparition.
Depuis que les virus sont connus (il a fallu attendre les années 1920-1930), deux pandémies majeures de grippe A ont existé au XXe siècle, la grippe « asiatique » de 1956-1958, de type A (H2N2) et la grippe de Hong Kong, de 1968-1970, de type A (H3N2). Ces deux pandémies ont fait environ 1 millions de morts pour la première, et entre 2 et 4 millions de morts pour la seconde. La presse a beaucoup parlé de la grippe asiatique mais beaucoup moins de la grippe de Hong Kong. Moi-même, qui avait entre 18 et 20 ans à l’époque, je n’en ai aucun souvenir. Cela s’explique en grande partie par le contexte politique de l’époque. On était encore dans la période des Trente Glorieuses, période assez euphorique pour la jeunesse, et la politique internationale mobilisait fortement l’attention : l’après Mai 68 en France, l’après Printemps de Prague en Tchécoslovaquie, la guerre du Vietnam entre autres. Et puis, il faut bien le dire, l’espérance de vie n’était pas ce qu’elle est aujourd’hui. Au-delà de 65 ans, les gens étaient déjà classés parmi les vieillards.
Néanmoins, avec le recul, on s’est aperçu, alors que les pandémies de grippe étaient connues pour faire principalement des victimes chez les enfants en très bas âge et chez les personnes âgées, que cette fois, bien d’avantage que lors de la grippe asiatique de la décennie précédente, le taux de mortalité chez les personnes âgées, était nettement plus faible. Ce qui suggérait que des personnes âgées avaient sans doute déjà été exposées précédemment à l’antigène H3 dans un passé lointain.
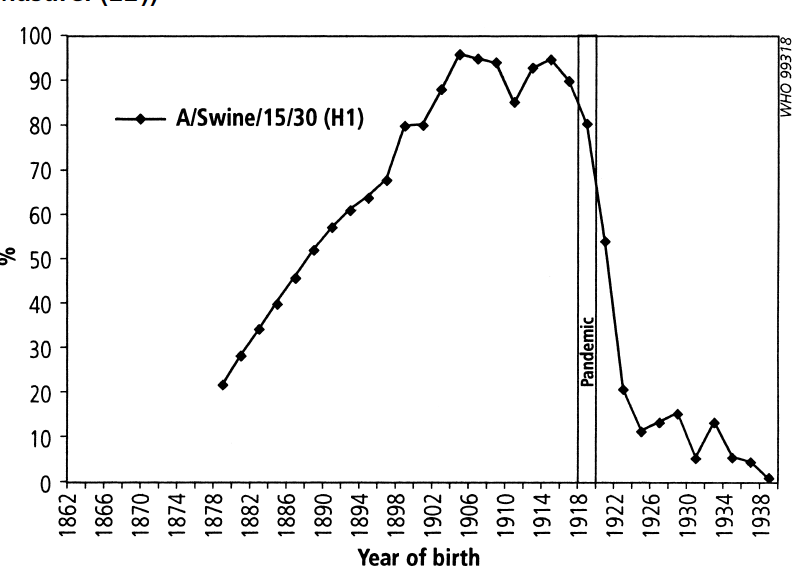
On peut déterminer cette date avec une bonne approximation en utilisant une méthode dite de « séroarchéologie ». Puisqu’il a très bien été documenté par ailleurs que la grande pandémie de grippe espagnole de 1918-1921 était due au sous-type A(H1N1), on a pu valider cette approche en utilisant un virus de cygne possédant l’hémagglutinine H1, et en mesurant le niveau d’inhibition de H1 (HI) par des sérums de personnes d’âges divers, collectés en 1967. On s’aperçoit alors qu’il faut remonter à des personnes nées 1924 pour voir un inhibition notable de H1, et que pour des personnes plus âgées, le taux d’inhibition monte brusquement pour atteindre un maximum chez des personnes nées en 1914, suivi d’un plateau jusqu’aux naissances en 1906, et ensuite une descente graduelle jusqu’en 1878 (échantillons les plus anciens ayant pu être prélevés), ceci étant du certainement à une immunité moindre développée chez des personnes plus âgées lors de la pandémie de 1918-1921. Mais ces résultats valident bien que cette technique de séroarchéologie permet de dater l’apparition de la pandémie dans les toutes premières années suivant le pic de présence d’anticorps neutralisant H1.
De façon similaire, des hémagglutinines H3 de la grippe de Hong Kong de 1968-1970 ont été mises en présence de sérums de personnes âgées de 30 ans ou plus en 1968, et aucune inhibition n’est observée en remontant jusqu’à des personnes nées en 1897. On voit ensuite apparaître une augmentation très raide de l’inhibition de H3, avec un maximum atteint pour des personnes nées en 1886, suivi d’un plateau jusqu’à 1870 et ensuite une descente lente jusqu’en 1862, date de naissance la plus lointaine pour laquelle on a pu disposer d’échantillons de sang.
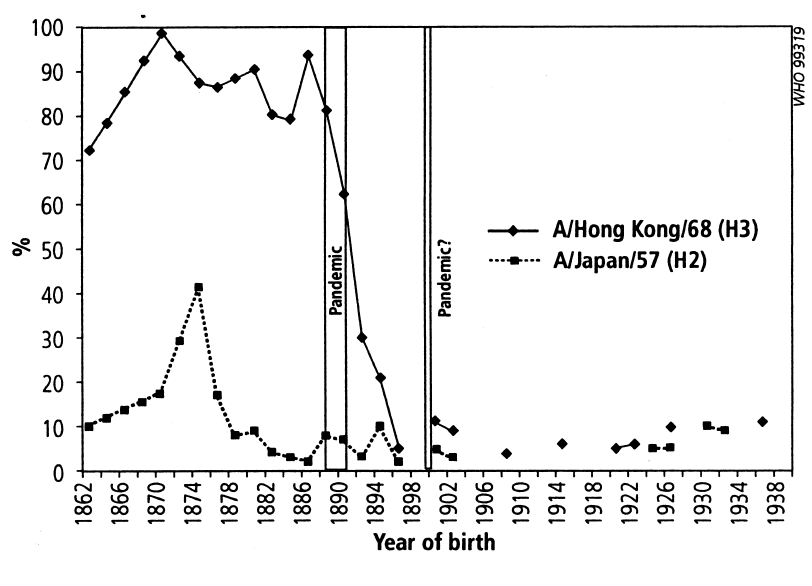
En comparaison avec l’analyse faite pour la pandémie A(H1N1) de la grippe espagnole, on arrive ainsi à la conclusion qu’il y a eu une éclosion de virus à hémagglutinine H3 vers 1889, ce qui correspond à l’apparition de la grippe russe.
Par une méthode similaire, il a pu être déterminé que la neuraminidase N de ce virus était du sous-type N8, et que le nouveau virus grippal émergeant à ce moment était le sous-type A(H3N8) et non pas le sous-type A(H3N2) de la pandémie de 1968-1970. Néanmoins, les personnes âgées de plus de 75 ans avait déjà été exposées à l’hémagglutinine H3, et profitaient donc encore d’une assez bonne immunité, ce qui pouvait expliquer une mortalité plus faible qu’attendue, si on compare par exemple avec la grippe asiatique de la décennie précédente.
Arguments en faveur d’une pandémie à coronavirus
Nous connaissons à ce jour 7 coronavirus humains. Bien évidemment celui qui est responsable de la pandémie en cours, le SARS-CoV-2, qui est apparu à Wuhan, dans la province chinoise de Hubei en fin d’année 2019. Pour cette raison, la maladie associée à ce virus a été appelée « COronaVIrus Disease from 2019 », autrement dite Covid-19.
Mais avant cela, deux autres coronavirus apparurent soudainement, contagieux, causant des syndromes respiratoires aigus comme le SARS-CoV-2, et mortels dans un certain nombre de cas. Ce fut d’abord le SARS (pour « Severe Acute Respiratory Syndrome »), apparu en Chine, dans la province du Guangdong, et qui a sévit de 2002 à 2004, en se dispersant dans le monde, mais qui fort heureusement n’a pas réussi à s’accrocher, les foyers s’étant éteints rapidement sans se transformer en une pandémie. Plus tard, à l’apparition du virus de 2019, ce virus du SARS a été rebaptisé SARS-CoV ou Sars-CoV-1.
De même, en 2012, est apparu un autre coronavirus au Moyen-Orient, pouvant aussi provoquer des syndromes respiratoires sévères aigus, sous forme de pneumonies, et qui a sévit au Moyen-Orient de 2012 à 2014, mais lui aussi, en restant relativement localisé, et donc en ne se transformant pas non plus en pandémie. Il fut baptisé MERS ou MERS-CoV pour « Middle East Respiratory Syndrome-related coronavirus ».
Mais bien avant ça, il existait déjà 4 autres coronavirus circulant parmi l’espèce humaine. Ce sont les coronavirus 229E, NL63, OC43 et HKU1. OC43 et 229E semblent les plus répandus et sont en général responsables de rhumes bénins, bien qu’en de rares occasions, ils aient provoqué des complications bronchiques et pulmonaires plus sérieuses chez des personnes âgées ou souffrant de comorbidités. Ils ont été pour la première fois identifiés dans les années ’60. Ces deux coronavirus sont responsables d’environ 30% des rhumes bénins. Les deux autres, NL63 et HKU1 semblent plus rares. Ils ont été identifiés seulement vers le milieu des années 2000, lors d’affections respiratoires sérieuses chez des enfants comme chez des personnes âgées.
Tous les coronavirus sont des virus à ARN monocaténaires, donc, comme pour la grippe, formé d’un seul brin d’ARN. Mais contrairement à la grippe, l’ARN n’est pas fragmenté, mais est formé d’une fibre d’ARN d’un seul tenant. Les coronavirus sont d’ailleurs les virus à ARN connu, possédant le plus long génome à ARN. En outre, l’ARN des coronavirus, toujours par opposition avec la grippe, est à polarité positive, c’est à dire qu’il peut être lu par les ribosomes directement, sans devoir être répliqué préalablement en ARN complémentaire.
En principe donc, les coronavirus ont moins de chance de muter que les virus de grippe. C’est ce qui semble en réalité se produire, bien que le génome monocaténaire d’ARN soit beaucoup moins stable qu’un ADN bicaténaire, et que les mutations sont encore très fréquentes.
Lors de l’épidémie de SARS de 2003, le monde était sous surveillance étroite. Et donc, quand une flambée de cas s’est soudainement déclenchée dans une maison de repos pour personnes âgées au Canada, en Colombie Britannique, avec 95 résidents atteints sur 142 et 53 membres du personnel sur 160, avec fièvre, toux, pneumonies dans 12% des cas, et décès de huit résidents, on a immédiatement pensé à un foyer de SARS. Les tests PCR spécifiques du SARS s’avéraient cependant négatifs, même après avoir été répétés. Des tests PCR spécifiques d’autres coronavirus ont alors été entrepris, et il s’est avéré que dans ce cas, il s’agissait d’un foyer d’une forme particulièrement virulente du virus HCoV-OC43, le plus souvent bénin.
Cette épidémie de SARS, et également ce cas particulièrement intense de foyer de OC43 a amené la communauté scientifique à s’intéresser de beaucoup plus près aux coronavirus, des agents pathogènes que la médecine avait jusque-là assez fort négligés. En 2005, l’équipe universitaire de la KULeuven en Belgique, dirigée par le Professeur Marc Van Ranst, a effectué le séquençage complet du OC43 et a montré un très haut degré de similitude avec le coronavirus bovin BCoV qui avait déjà été séquencé auparavant, allant de 93% pour la protéine Spike jusqu’à 98% pour la protéine E de l’enveloppe. En se basant sur ces similitudes, ils sont arrivés à la conclusion que BCoV et OC43 devaient avoir un ancêtre commun. En analysant l’évolution des mutations de ces deux virus, une première fois en 2005, puis de façon plus précise en 2006, en se basant sur 9 échantillons de BCoV collectés entre 1965 et 1998, et 8 échantillons de OC43 collectés entre 1967 et 2004, ils ont calculé que le moment où les deux virus ont divergé l’un de l’autre à partir d’un ancêtre commun, devait se situer dans la dernière décennie du XIXe siècle. Ceci serait donc aussi en convergence avec l’émergence d’un nouveau coronavirus humain HCoV-OC43 à la fin du XIXe siècle, lequel pourrait donc également être le pathogène de la pandémie de grippe russe.
En août 2020, une équipe danoise dirigée par les Dr. Lone Simonsen et Anders Gorm Pedersen, a même affirmé avoir pu affiner davantage les résultats, en disposant de plus de 30 souches de HCoV-OC43 de rhume humain collectés au cours des 15 dernières années. Ils ont donc pu calculer la fréquence de mutation de ce virus, et de là, extrapoler le moment où celui-ci a commencé à se distinguer du virus bovin. Ils sont arrivés à la même conclusion que l’équipe belge : le HCoV‑OC43 se serait séparé du virus bovin et aurait franchi la barrière des espèces vers 1890. Fort malheureusement, jusqu’ici, cette équipe n’a pas encore formellement publié ses résultats.
Pandémie de 1889 : Grippe A(H3N8) ou Coronavirus HCoV-OC43 ?
La grippe espagnole de 1918-1921 est très bien documentée, car de nombreux chercheurs ont continué à y travaillé jusqu’à cette dernière décennie. À l’époque toutefois, la couverture médiatique ne fut pas extraordinaire, bien moindre que pour la grippe russe. D’abord parce que les deux premières vagues, la première au printemps 1918, qui fut relativement légère et limitée au front, et la seconde à l’été et l’automne 1918, qui fut extrêmement meurtrière, furent soumises à la censure des pays belligérants, alors que l’Espagne, durement touchée, mais neutre, en fit abondamment mention dans la presse, si bien que beaucoup crurent que cette grippe venait d’Espagne, alors qu’elle fut importées par les troupes américaines, vraisemblablement à partir d’un camp situé dans le Kansas. La pandémie a encore connu une troisième vague en Europe en 1919, puis a très fortement diminué en intensité, tandis qu’elle a continué dans d’autres parties du monde jusqu’en 1921.
On sait maintenant que le nombre de victimes annoncées à l’époque, de l’ordre de 10 à 20 millions de morts, était largement sous-estimé, mais que cette pandémie ultra-meurtrière à fait entre 50 et 100 millions de victimes (l’imprécision vient des difficultés de recensement dans les grands espaces russes et chinois, où les registres de populations étaient pratiquement inexistants), et que l’agent responsable était sans aucun doute possible le virus grippal A(H1N1) puisqu’on a pu reconstituer en 2008 son ADN à partir de lambeaux de poumons de cadavres enfouis dans le permafrost d'un cimetière d’une cité du nord de l’Alaska où la totalité des habitants étaient morts de la grippe espagnole. Ce virus a été entièrement reconstitué en laboratoire, laboratoire ultra-sécurisé, fort heureusement.
Il ne sera jamais possible d’obtenir une telle certitude à propos de l’agent causal de la pandémie de 1889. Retrouver des cadavres dans un état de conservation suffisant est impossible pour une période aussi lointaine, le nombre de victimes était beaucoup plus faible, et on ne dispose d’aucune donnée indiquant la présence d’un cimetière du type évoqué plus haut dans le grand nord.
Or ni la séroarchéologie utilisée pour justifier H3, ni l’horloge moléculaire utilisant les mutations de BCoV et de HCoV-OC43 ne sont des preuves de causalité. Et si l’apparition de H3 (ou sa réapparition) est possible par le simple jeu des réarrangements de l’ARN grippal avec un virus animal (aviaire dans la plupart des cas), il convient d’analyser de plus près quels sont les arguments en faveur de l’émergence d’un coronavirus humain pandémique à cette époque.
Une première chose à mettre en évidence, si on compare avec SARS-CoV-2, c’est que les enfants en bas âge étaient peu touchés, ou en tous cas ne présentaient que des symptômes faibles, alors que les personnes plus âgées constituaient la majorité des victimes. C’est aussi le cas pour le Covid-19, alors que les cas graves de grippe se manifestent à la fois chez les personnes âgées et chez les enfants en très bas âge.
La maladie s’attaquait aussi à des organes variés, principalement le système respiratoire, gastro-intestinal (diarrhées et vomissements) et au système nerveux (notamment des maux de tête importants sur la partie frontale, qui pouvaient durer très longtemps, et des pertes de goût et d’odorat étaient aussi signalés), ainsi qu’au système cardiovasculaire, puisque de nombreux cas de thromboses ont été signalé, conduisant parfois à des embolies pulmonaires.
Mais surtout, on sait qu’au XIXe siècle, une maladie respiratoire très infectieuse a affecté le bétail du monde entier, avec une mortalité très importante, principalement entre 1870 et 1890. Ces épidémies bovines ont conduit à des abattages en masse, exposant donc de nombreux travailleurs du secteur aux agents pathogènes responsables. En ce siècle d’industrialisation, la population européenne augmentait rapidement. La Grande Bretagne passa de 11 millions de citoyens en 1801 à 21 millions en 1851. Les transports humains et de denrées étaient de plus en plus nombreux avec les colonies. Or à cette époque, on n’en était encore qu’aux balbutiements du chemin de fer et de la navigation à vapeur, et tous déplacements sur de longues distances étaient longs. La congélation des aliments n’existait évidemment pas. Dans les campagnes, les habitants pouvaient se procurer leur lait grâce à quelques têtes de bétail. Mais dans les villes, de plus en plus peuplées du fait de l’industrialisation, il n’y avait guère d’autre moyen pour nourrir la population, que d’amener les bovins vivants, disséminant ainsi rapidement leur maladie à travers le monde.
Il est très vraisemblable que l’agent pathogène ait été alors l’ancêtre du virus bovin BCoV. De plus, il est bien connu aujourd’hui que ce virus peut passer et s’adapter à un grand nombre d’espèces telles que le cheval et le chien. Et on a même décelé, depuis que la RT-PCR a fait son apparition, de rares cas de diarrhées chez l’enfant, où le BCoV était le facteur causal. Un grand ensemble de facteurs, détaillés dans des rapports cliniques britanniques et allemands de l’époque, vont ainsi dans le sens d’un passage vers cette époque du BCoV à l’homme, chez qui il se serait adapté pour se transformer en le premier coronavirus humain identifié dans les années 1960 : HCoV-OC43.
Propagation de la première vague de la pandémie de 1889 à travers le monde.
La pandémie a commencé à se manifester vers novembre-décembre 1889, en provenance de l’Est, des environs de Boukhara (à l’époque Turkestan, aujourd’hui Ouzbékistan), et pour cette raison, fut appelée « Grippe russe ». Après être restée localisée dans le centre de l’Asie pendant 6 mois, elle apparaît en octobre dans diverses villes russes, dont Moscou et Saint-Pétersbourg avant de se répandre dans le reste de l’Europe. Elle s’est répandue en plusieurs vagues successives en 1889-1890, printemps 1891, 1891-1892, très meurtrière, et sans doute jusqu’au printemps 1895.

Cette pandémie a été très bien documentée, non seulement grâce à un rapport détaillé établi par le Dr Parsons pour le gouvernement britannique (1891), mais aussi dans la presse quotidienne. La grippe russe est documentée dans la presse anglaise (The Times), allemande (Vossische Zeitung), française (Le Monde) ou encore polonaise (surtout à Poznán, à l’époque sous contrôle prussien).
À Saint-Pétersbourg, on dénombra environ 150.000 personnes touchées en décembre 1889, dont le Tsar. 50% des enfants en âge scolaire furent contaminés. 200.000 cas furent recensés à Moscou. Toujours en décembre, des villes comme Copenhague, Vienne et Paris furent touchées. En janvier 1890, le virus atteint la Méditerranée, la Grande Bretagne et les Etats-Unis. En janvier également, le Tsar est touché une seconde fois.
À Paris, au mois de décembre 1889, les hôpitaux sont vites débordés. La grippe se transforme rapidement en une épidémie de pneumonie, et on compte 200 morts de plus chaque semaine, si bien que des hôpitaux de campagne doivent être créés dans l’urgence, les structures hospitalières ne pouvant plus suivre. Vers le 28 décembre, l’épidémie semble perdre en intensité à Paris mais gagne dans les autres grandes villes. Des villes comme Toulon, Ajaccio, Grenoble sont fortement touchées. Les universités de Montpellier et d’Angers doivent fermer, ainsi que toutes les écoles et l’opéra de Lyon. À l’Hôtel-Dieu, tous les médecins développent la maladie. La mortalité est estimée à 30% supérieure aux années précédentes, toutes causes confondues. Toujours à Paris, la presse parle de 400 à 500 cérémonies funèbres par jour, du jamais vu depuis la guerre de 1870. Très vite, l’économie s’en ressent. Les boulangers et les bouchers vendent des centaines de kg de nourriture en moins. Lyon doit arrêter ses métiers à tisser. Les villes de Marseille, Bordeaux, Rouen sont touchées à leur tour. De nombreux membres du gouvernement tombent malade. Puis, à la fin du mois de janvier, la presse ne parle presque plus de la maladie, comme si elle était en nette régression. IL est aussi noté que, contrairement à la grippe classique, un élargissement de la rate est notée dans de nombreux cas.
L’Italie et l’Espagne sont également gravement touchées. En décembre 1889, on dénombre 52000 cas à Madrid et un très grand nombre de morts. En janvier, à Madrid comme à Barcelone, on dénombre 200 à 300 morts par jour. Les gens pauvres n’ont plus rien pour se chauffer, et presque rien à manger.
En Allemagne et en Autriche, le nombre de cas augmente très rapidement en décembre. On dénombre jusqu’à 150.000 cas à Berlin. Là aussi, petit à petit, les pneumonies sont de plus en plus nombreuses et les morts s’accumulent.
À Londres, l’épidémie commence surtout à frapper en janvier 1890. On dénombre 1070 morts de pneumonie. Et très vite l’épidémie se répand dans les autres villes, jusqu’à Glasgow, Edinburgh et Dublin.
Les journaux de Poznań, qui ont le mieux décrit la progression de l’épidémie, parlent peu des autres villes. Néanmoins, ils mentionnent la présence de la maladie en Sicile, en Grèce, à New York, d’où elle s’étend sur tout le territoire.
En février, l’épidémie semble reculer, et en mars, il semble qu’elle ait pratiquement fini de sévir.
Sur le plan clinique, on a surtout observé :
- Maladie plus contagieuse que la grippe,
- Doigts gonflés en début de maladie (vascularite ? c’est-à-dire inflammation des parois des vaisseaux), thromboses et embolies pulmonaires,
- Atteintes sévères plus fréquentes chez l’homme,
- Atteintes rénales et digestives,
- Mortalité plus élevée chez les personnes âgées (notion de comorbidité inconnue),
- Récidives rapides chez 15% des patients (ce qui reste exceptionnel semble-t-il pour le Covid 19),
- Perte de goût et d’odorat,
- Manifestations neurologiques anormalement élevées pour une grippe, faisant dire au Pr Pierre Potain (connu pour ses travaux sur la pression artérielle) que cette grippe n’est pas la grippe
Nul ne peut affirmer que la pandémie née en 1889 était une pandémie de coronavirus plutôt que de grippe, malgré que la rapidité de propagation, suggérant une très faible immunité de la population, y compris chez les personnes qui avaient connu les dernières épidémies importantes de la décennie 1840. À cela s’ajoute surtout une série de symptômes décrits ci-dessus, dont certains, comme les problèmes neurologiques, dont la perte de goût et d’odorat, et les problèmes vasculaires. Des symptômes qui sont à rapprocher de symptômes observés lors de la pandémie actuelle de Covid-19.
Un regain d’attention sur la grippe russe se reflète d’ailleurs dans la littérature scientifique de cette dernière année, pour essayer de mieux comprendre cette pandémie qui a débuté en 1889, malheureusement en l’absence d’éléments matériels, pour tenter de confirmer ou d’infirmer qu’il s’agissait bien d’une première pandémie à coronavirus, et le cas échéant, d’en tirer des leçons.Il n’est d’ailleurs pas exclu que deux pathogènes nouveaux aient circulé en même temps, ou que la grippe A(H3N8) ait été responsables des épisodes de grippe qui ont immédiatement suivi. Il est vraisemblable qu’on ne puisse apporter de réponse définitive dans un avenir proche.
Références
W.R. Dowdle, Influenza A virus recycling revisited, Bull. Wld Hlth Org., 1999, 77(10), 820-828.
A. Knapp, The secret history of the first coronavirus, Forbes, 11th Apri 2020
Vidal, Pandémie de grippe russe : un Covid du XIXe siècle ?, 26 novembre 2020